Câu hỏi Tốc độ phản ứng và cân bằng hóa học
Danh sách câu hỏi
[Một phản ứng thuận nghịch ở trạng thái cân bằng thì tốc độ p - Luyện Tập 247] Một phản ứng thuận nghịch ở trạng thái cân bằng thì tốc độ phản ứng thuận (vt) bằng tốc độ phản ứng nghịch (vn). Khi thay đổi các yếu tố nồng độ, áp suất, nhiệt độ… thì có thể xẩy ra các trường hợp sau:
1. vt tăng, vn giảm
2. vt và vn đều giảm nhưng vn giảm nhiều hơn vt
3. vt và vn đều tăng nhưng vn tăng nhiều hơn vt
4. vn tăng, vt không đổi
5. vn và vt đều không đổi
Trong số các trường hợp trên, có bao nhiêu trường hợp làm cân bằng dịch chuyển theo chiều thuận
[Cho các cân bằng hóa học sau: (a) H<sub>2</sub> (k) + I<sub - Luyện Tập 247] Cho các cân bằng hóa học sau:
(a) H2 (k) + I2 (k)
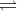 2HI (k). (b) 2NO2 (k)
2HI (k). (b) 2NO2 (k) 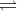 N2O4 (k).
N2O4 (k). (c) 3H2 (k) + N2 (k)
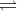 2NH3 (k). (d) 2SO2 (k) + O2 (k)
2NH3 (k). (d) 2SO2 (k) + O2 (k) 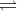 2SO3 (k).
2SO3 (k).Ở nhiệt độ không đổi, khi thay đổi áp suất chung của mỗi hệ cân bằng, cân bằng hóa học nào ở trên không bị chuyển dịch?
[Cho các cân bằng hóa học sau: (a) H<sub>2</sub> (k) + I<sub - Luyện Tập 247] Cho các cân bằng hóa học sau:
(a) H2 (k) + I2 (k)
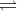 2HI (k). (b) 2NO2 (k)
2HI (k). (b) 2NO2 (k) 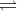 N2O4 (k).
N2O4 (k). (c) 3H2 (k) + N2 (k)
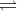 2NH3 (k). (d) 2SO2 (k) + O2 (k)
2NH3 (k). (d) 2SO2 (k) + O2 (k) 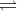 2SO3 (k).
2SO3 (k).Ở nhiệt độ không đổi, khi thay đổi áp suất chung của mỗi hệ cân bằng, cân bằng hóa học nào ở trên không bị chuyển dịch?
[Cho cân bẳng hóa học ( trong bình kín) sau: N<sub>2</sub>(kh - Luyện Tập 247] Cho cân bẳng hóa học ( trong bình kín) sau: N2(khí) + 3H2(khí) 2NH3 ΔH= -92kJ/mol
Trong các yếu tố:
(1) Thêm một lượng N2 hoặc H2.
(2) Thêm một lượng NH3.
(3) Tăng nhiệt độ của phản ứng.
(4) Tăng áp suất của phản ứng.
(5) Dùng thêm chất xuc tác.
Có bao nhiêu yếu tố làm cho tỉ khối của hỗn hợp khí trong bình so với H2 tăng lên?
[Cho cân bằng hóa học sau (xảy ra trong bình kín dung tích kh - Luyện Tập 247] Cho cân bằng hóa học sau (xảy ra trong bình kín dung tích không đổi): PCl5 (k)↔PCl3 (k) + Cl2 (k); ∆H > 0
Trong các yếu tố:
(1) tăng nhiệt độ của hệ phản ứng;
(2) thêm một lượng khí Cl2;
(3) thêm một lượng khí PCl5;
(4) tăng áp suất chung của hệ phản ứng;
(5) dùng chất xúc tác.
Những yếu tố nào đều làm cân bằng chuyển dịch theo chiều thuận (giữ nguyên các yếu tố khác)?
[Xét phản ứng hoá học: A<sub>(khí)</sub><strong> +2B<sub>(k - Luyện Tập 247] Xét phản ứng hoá học: A(khí) +2B(khí) → C(khí) + D(khí). Tốc độ của phản ứng được tính theo biểu thức: v= k[A].[B]2, trong đó k là hằng số tốc độ phản ứng; [A] và [B] nồng độ mol/lít của các chất A, B tương ứng. Khi nồng độ của chất B tăng 3 lần, nồng độ của chất A giảm 6 lần thì tốc độ phản ứng so với trước là:
[Cho cân bằng hóa học sau: 2SO<sub>2</sub> (k) + O<sub>2</sub - Luyện Tập 247] Cho cân bằng hóa học sau: 2SO2 (k) + O2 (k) 2SO3 (k) ; DH < 0
Cho các biện pháp : (1) tăng nhiệt độ, (2) tăng áp suất chung của hệ phản ứng, (3) hạ nhiệt độ, (4)dùng thêm chất xúc tác V2O5, (5) giảm nồng độ SO3, (6) giảm áp suất chung của hệ phản ứng. Những biện pháp nào làm cân bằng trên chuyển dịch theo chiều thuận?
[Cho cân bằng: C<sub>(r) </sub>+ CO<sub>2(k) </sub><-> 2CO<s - Luyện Tập 247] Cho cân bằng: C(r) + CO2(k) 2CO(k). Ở 550oC , hằng số cân bằng KC của phản ứng trên bằng 2.10-3. Người ta cho 0,2 mol C và 1 mol CO2 vào bình kín dung tích 22,4 lít (không chứa không khí). Nâng dần nhiệt độ trong bình lên đến 550oC và giữ nhiệt độ đó để cho cân bằng được thiết lập. Số mol CO trong bình là
[Cho cân bằng trong bình kín : CO<sub>(k)</sub> + H<sub>2</s - Luyện Tập 247] Cho cân bằng trong bình kín :
CO(k) + H2O(k) CO2(k) + H2(k) DH < 0
Trong các yếu tố : (1) tăng nhiệt độ ; (2) thêm một lượng hơi nước ; (3) thêm một lượng H2 ; (4) tăng áp suất chung của hệ ; (5) thêm chất xúc tác.
Dãy gồm các yếu tố làm thay đổi cân bằng của hệ là :
[Cho cân bằng trong bình kín : CO<sub>(k)</sub> + H<sub>2</s - Luyện Tập 247] Cho cân bằng trong bình kín :
CO(k) + H2O(k) CO2(k) + H2(k) DH < 0
Trong các yếu tố : (1) tăng nhiệt độ ; (2) thêm một lượng hơi nước ; (3) thêm một lượng H2 ; (4) tăng áp suất chung của hệ ; (5) thêm chất xúc tác.
Dãy gồm các yếu tố làm thay đổi cân bằng của hệ là :
[Xét phân hủy N<sub>2</sub>O<sub>5</sub> trong dung môi CCl<s - Luyện Tập 247] Xét phân hủy N2O5 trong dung môi CCl4 ở 45oC: N2O5→N2O4 + 1/2O2. Ban đầu nồng độ của N2O5 là 2,33M, sau 184 giây nồng độ của N2O5 là 2,08M. Tốc độ trung bình của phản ứng tính theo N2O5 là:
[Cho 3 mẫu đá vôi (100CO<sub>3</sub>) có cùng khối lượng: - Luyện Tập 247] Cho 3 mẫu đá vôi (100%CaCO3) có cùng khối lượng: Mẫu 1 dạng khối, mẫu 2 dạng viên nhỏ, mẫu 3 dạng bột mịn vào 3 cốc đựng có cùng thể tích dung dịch HCl(dư, cùng nồng độ, ở điều kiện thường). Thời gian để đá vôi tan hết trong 3 cốc tương ứng là t1, t2 ,t3 giây. So sánh nào sau đây đúng?
[Cho 3 mẫu đá vôi (100CO<sub>3</sub>) có cùng khối lượng: - Luyện Tập 247] Cho 3 mẫu đá vôi (100%CaCO3) có cùng khối lượng: Mẫu 1 dạng khối, mẫu 2 dạng viên nhỏ, mẫu 3 dạng bột mịn vào 3 cốc đựng có cùng thể tích dung dịch HCl(dư, cùng nồng độ, ở điều kiện thường). Thời gian để đá vôi tan hết trong 3 cốc tương ứng là t1, t2 ,t3 giây. So sánh nào sau đây đúng?
[Cho khí HI vào 1 bình kín đun nóng đến nhiệt độ xác định thì - Luyện Tập 247] Cho khí HI vào 1 bình kín đun nóng đến nhiệt độ xác định thì xảy ra phản ứng :
2HI(k) H2(k) + I2(k) DH = -52 kJ
Trong các yếu tố sau : nồng độ ; nhiệt độ ; áp suất ; chất xúc tác . Số yếu tố ảnh hưởng đến chuyển dịch cân bằng là :