Cho 30 gam hỗn hợp gồm Al Cu và Zn tác dụng vừa đủ với

Câu hỏi và phương pháp giải
Nhận biếtCho 30 gam hỗn hợp gồm Al, Cu và Zn tác dụng vừa đủ với 712,5 ml dung dịch HNO3 2,0M, thu được dung dịch chứa m gam muối và 5,6 lít hỗn hợp khí X (đktc) gồm NO và N2O. Tỉ khối của X so với He là 8,2. Giá trị của m là
Đáp án đúng: D
Lời giải của Luyện Tập 247
Phương pháp giải:
- Các bán phản ứng nhận electron:
4H+ + NO3- + 3e → NO + 2H2O
10H+ + 2NO3- + 8e → N2O + 5H2O
10H+ + NO3- + 8e → NH4+ + 3H2O
- Công thức nhanh: nNO3-/muối KL = ne trao đổi
- m = mKL + mNO3-/muối KL + mNH4NO3
Giải chi tiết:
MX = 4.8,2 = 32,8 g/mol; nX = 5,6/22,4 = 0,25 mol.
Đường chéo:
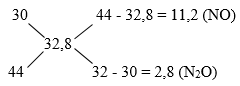
⟹ (left{ begin{array}{l}dfrac{{{n_{NO}}}}{{{n_{{N_2}O}}}} = dfrac{{11,2}}{{2,8}} = 4\{n_{NO}} + {n_{{N_2}O}} = 0,25end{array} right.) ⟹ (left{ begin{array}{l}{n_{NO}} = 0,{2^{mol}}\{n_{{N_2}O}} = 0,{05^{mol}}end{array} right.)
- Các bán phản ứng nhận electron:
4H+ + NO3- + 3e → NO + 2H2O (1)
0,8 ← 0,6 ← 0,2 (mol)
10H+ + 2NO3- + 8e → N2O + 5H2O (2)
0,5 ← 0,4 ← 0,05 (mol)
10H+ + NO3- + 8e → NH4+ + 3H2O (3)
nH+ = nHNO3 = 0,7125.2 = 1,425 mol.
⟹ nH+(3) = 1,425 - nH+(1) - nH+(2) = 0,125 mol.
⟹ nNH4NO3 = nNH4+ = nH+(3)/10 = 0,125/10 = 0,0125 mol.
Ta có: ne trao đổi = 3nNO + 8nN2O + 8nNH4+ = 3.0,2 + 8.0,05 + 8.0,0125 = 1,1 mol.
nNO3-/muối KL = ne trao đổi = 1,1 mol.
⟹ m = mKL + mNO3-/muối KL + mNH4NO3 = 30 + 1,1.62 + 0,0125.80 = 99,2 gam.
Đáp án D