Toggle Mobile Menu
Hòa tan hoàn toàn 20 gam hỗn hợp X gồm Mg Fe2O3 bằng dung dịch H2SO4 loãng dư thấy thoát ra V lít H2

Câu hỏi và phương pháp giải
Nhận biếtHòa tan hoàn toàn 20 gam hỗn hợp X gồm Mg, Fe2O3 bằng dung dịch H2SO4 loãng dư thấy thoát ra V lít H2 (đktc) và thu được dung dịch Y. Thêm từ từ NaOH đến dư và dung dịch Y. Kết thúc thí nghiệm, lọc lấy kết tủa đem nung trong không khí đến khối lượng không đổi thu được 28 gam chất rắn. Giá trị của V là:
Đáp án đúng: B
Lời giải của Luyện Tập 247
Giải chi tiết:
Mg 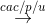 MgO
MgO
Fe2O3 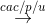 Fe2O3
Fe2O3
=> mTăng = mO (MgO) = 28 – 8 = 8 gam
Suy ra: nMgO = 0,5 mol , 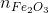 = 0,05 mol
= 0,05 mol
Fe2O3 + H2SO4 → Fe2(SO4)3 + H2O
0,05 → 0,05
Mg + Fe2(SO4)3 → MgSO4 + 2FeSO4 (Tính oxi hóa Fe3+ > H+)
0,05 ← 0,05
Mg + H2SO4 → MgSO4 + H2
=> nMg (phản ứng với axit) = 0,5 – 0,05 = 0,45 (mol)
=> V = 0,45. 22,4 = 10,08 lít