Trong bình kín chứa 05 mol CO và m gam Fe3O4 Sau một th

Câu hỏi và phương pháp giải
Nhận biếtTrong bình kín chứa 0,5 mol CO và m gam Fe3O4. Sau một thời gian nung nóng bình, thu được 28,4 gam chất rắn X và hỗn hợp khí Y trong bình có tỉ khối so với khí H2 bằng 20,4. Nhận định nào sau đây đúng?
Đáp án đúng: D
Lời giải của Luyện Tập 247
Phương pháp giải:
Đây là quá trình khử Fe3O4 ⟹ Sản phẩm không thể có Fe2O3 (do số oxi hóa Fe trong Fe2O3 lớn hơn số oxi hóa Fe trong Fe3O4).
Giải chi tiết:
- Đây là quá trình khử Fe3O4 ⟹ Sản phẩm không thể có Fe2O3 (do số oxi hóa Fe trong Fe2O3 lớn hơn số oxi hóa Fe trong Fe3O4).
- MY = 2.10,2 = 20,4 g/mol, hỗn hợp khí Y gồm CO2 và CO dư.
⟹ nCO + ({n_{C{O_2}}}) = 0,5 (1)
Ta có đường chéo:
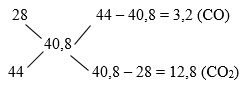
⟹ nCO/({n_{C{O_2}}}) = 1/4 (2)
Từ (1)(2) ⟹ nCO = 0,1 mol; ({n_{C{O_2}}}) = 0,4 mol.
⟹ nO mất đi = ({n_{C{O_2}}}) = 0,4 mol.
⟹ ({m_{F{e_3}{O_4}}}) = mX + mO mất đi = 28,4 + 0,4.16 = 34,8 gam.
Đáp án D