Cho hai hệ cân bằng sau trong hai bình kín: C (r) + CO2 (k) <

Câu hỏi và phương pháp giải
Nhận biếtCho hai hệ cân bằng sau trong hai bình kín:
C (r) + CO2 (k) 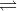 2CO(k) ;
2CO(k) ; 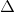 H = 172 kJ
H = 172 kJ
CO (k) + H2O (k) 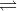 CO2 (k) + H2 (k) ;
CO2 (k) + H2 (k) ; 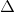 H = - 41 kJ
H = - 41 kJ
Có bao nhiêu điều kiện trong các điều kiện sau đây làm các cân bằng trên chuyển dịch ngược chiều nhau (giữ nguyên các điều kiện khác)?
(1) Tăng nhiệt độ.
(2) Thêm khí CO2 vào.
(3) Thêm khí H2 vào.
(4) Tăng áp suất.
(5) Dùng chất xúc tác.
(6) Thêm khí CO vào
Đáp án đúng: D
Lời giải của Luyện Tập 247
Giải chi tiết:
kí hiệu pt 1 là I và pt 2 là II, ta có:
(1) Tăng nhiệt độ thì cân bằng (I) chuyển dịch theo chiều thuận còn (II) chuyển dịch theo chiều nghịch.
(2) Thêm khí CO2 thì cân bằng (I) chuyển dịch theo chiều thuận còn (II) chuyển dịch theo chiều nghịch.
(3) thêm khí H2 thì cả cân bằng (I) không chuyển dịch, còn (II) chuyển dịch theo chiều nghịch.
(4) Tăng áp suất thì cân bằng (I) chuyển dịch theo chiều nghịch còn cân bằng (II) không chuyển dịch.
(5) Dùng chất xúc tác thì cả hai cân bằng không chuyển dịch.
(6) Thêm khí CO thì cân bằng (I) chuyển dịch theo chiều nghịch còn (II) chuyển dịch theo chiều thuận.
=> Bao gồm các điều kiện (1), (2) và (6).
( * ) Xem thêm: Ôn tập luyện thi thpt quốc gia môn hóa cơ bản và nâng cao. Tổng hợp đầy đủ lý thuyết, công thức, phương pháp giải và bài tập vận dụng.