Oxi hóa hoàn toàn 46 gam chất hữu cơ D bằng CuO đun nóng ở nhiệt độ cao. Sau phản ứng thu được 448 l

Câu hỏi và phương pháp giải
Nhận biếtOxi hóa hoàn toàn 4,6 gam chất hữu cơ D bằng CuO đun nóng ở nhiệt độ cao. Sau phản ứng thu được 4,48 lít khí CO2( đktc) và nước, đồng thời thấy khối lượng chất rắn thu được giảm 9,6 gam so với khối lượng của CuO ban đầu. Xác định công thức phân tử của D. Xác định công thức cấu tạo có thể có của D.
Đáp án đúng: A
Lời giải của Luyện Tập 247
Giải chi tiết:
Khối lượng chất rắn giảm 9,6 gam so với khối lượng CuO ban đầu chính là khối lượng oxi do CuO phân hủy để đốt cháy 4,6g chất D.
Số mol CO2 = (4,48 : 22,4) = 0,2 mol
=>Khối lượng CO2 = 0,2. 44 = 8,8 gam
Sơ đồ phản ứng:
D + O2 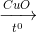 CO2 + H2O
CO2 + H2O
4,6g → 9,6g → 8,8 g → 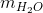
Suy ra: Khối lượng CO2 + Khối lượng H2O = mD + 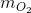
Khối lượng nước = 4,6 + 9,6 – 8,8 = 5,4 gam
Suy ra:
mC = 12. 0,2 = 2,4 gam
mH = 2. 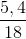 = 0,6 gam
= 0,6 gam
nH = 0,6 mol
mO = 4,6 – ( 2,4 + 0,6 ) = 1,6 gam
nO = 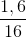 = 0,2 mol
= 0,2 mol
suy ra: nC : nH : nO = 0,2 : 0,6 : 0,1 = 2: 6: 1
Công thức phân tử dạng (C2H6O)n
Điều kiện:
nH ≤ 2nC + 2 ó 6n ≤ 2.2n + 2 => n ≤ 1
Vậy n = 1 => CTPT C2H6O
CTCT là CH3 – CH2 – OH (rượu etylic)
CH3 – O – CH3 (đimetyl ete)