Cho phương trình hóa học tổng hợp amoniac : N2 +

Câu hỏi và phương pháp giải
Nhận biếtCho phương trình hóa học tổng hợp amoniac : N2 + 3H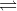 2 2NH3 (∆H < 0) . Khi phản ứng đạt trạng thái cân bằng thì tỉ khối của hỗn hợp khí trong bình so với H2 là d1 ; Đun nóng bình sau 1 thời gian phản ứng đạt tới trạng thái cân bằng mới thì tỉ khối lúc này so với H2 là d2 . So sánh d1 và d2 ta thấy:
2 2NH3 (∆H < 0) . Khi phản ứng đạt trạng thái cân bằng thì tỉ khối của hỗn hợp khí trong bình so với H2 là d1 ; Đun nóng bình sau 1 thời gian phản ứng đạt tới trạng thái cân bằng mới thì tỉ khối lúc này so với H2 là d2 . So sánh d1 và d2 ta thấy:
Đáp án đúng: B
Lời giải của Luyện Tập 247
Lời giải chi tiết:
Do cân bằng có ∆H phản ứng tỏa nhiệt theo chiều thuận
Khi đun nóng => Hệ sẽ thu nhiệt ; khi đó cân bằng sẽ chuyển dịch theo chiều nghịch
=> tổng số mol các chất trong hỗn hợp tăng nhưng do khối lượng không thay đổi nên khối lượng mol trung bình giảm => tỉ khối với H2 giảm
=> d1 > d2
=>B
( * ) Xem thêm: Ôn tập luyện thi thpt quốc gia môn hóa cơ bản và nâng cao. Tổng hợp đầy đủ lý thuyết, công thức, phương pháp giải và bài tập vận dụng.