Hòa tan hết m gam hỗn hợp ba oxit của sắt vào dung dịch HCl thu được dung dịch X. Cô cạn dung dịch X

Câu hỏi và phương pháp giải
Nhận biếtHòa tan hết m gam hỗn hợp ba oxit của sắt vào dung dịch HCl thu được dung dịch X. Cô cạn dung dịch X được m1 gam hỗn hợp 2 muối (có tỉ lệ mol 1 : 1). Mặt khác, nếu sục thật chậm khí clo đến dư vào dung dịch X, khi phản ứng kết thúc đem cô cạn dung dịch thì thu được (m1 + 1,42) gam muối khan. Hãy tính giá trị của m.
Đáp án đúng: A
Lời giải của Luyện Tập 247
Giải chi tiết:
Gọi x, y, z lần lượt là số mol FeO, Fe3O4, Fe2O3 trong m gam X.

Theo sơ đồ phản ứng và bài ra, ta có:
x + y = 2(y + z) (I)
Dựa vào sự tăng giảm số mol nguyên tử clo khi chuyển từ hỗn hợp X thành FeCl3, ta có:
Số mol nguyên tử clo tăng = Số mol FeCl2 trong X. Do đó:
=> (x + y) = 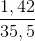 = 0,04 mol (II)
= 0,04 mol (II)
Từ (I) => (y + z ) = (x + y)/2 = 0,02 mol
=> Khối lượng m của các oxit:
m = mcác oxit = mFe + mO
= 56 (x + 3y + 2z ) + 16 ( x + 4y + 3z)
= 56 [ (x + y) + 2 ( y+ z)] + 16 [( x + y) + 3(y+z)]
= 56 ( 0,04 + 2. 0,02) + 16 ( 0,04 + 3. 0,02)
= 6,08 gam.