Hỗn hợp A gồm 64% Fe2O3 348% Fe 12% C. Cần bao nhiêu kg hỗn hợp A trộn với 1 tấn gang chứa 36% C còn

Câu hỏi và phương pháp giải
Nhận biếtHỗn hợp A gồm 64% Fe2O3, 34,8% Fe, 1,2% C. Cần bao nhiêu kg hỗn hợp A trộn với 1 tấn gang chứa 3,6% C, còn lại là Fe, để luyện được 1 loại thép chứa 1,2% C trong lò Mactanh. Biết các phản ứng xảy ra hoàn toàn. C bị oxi hóa thành cacbon oxit do Fe2O3 trong quá trình luyện thép.
Đáp án đúng: B
Lời giải của Luyện Tập 247
Giải chi tiết:
Theo đầu bài ta có phương trình hóa học:
Fe2O3 + 3C → 2Fe + 3CO (1)
Gọi số kg hỗn hợp A cần trộn là m do đó có:
mC = 0,012m (kg)
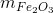 = 0,64 (kg)
= 0,64 (kg)
Khi trộn m kg hỗn hợp A với 1 tấn gang (1000 kg gang) ta có:
mC = 0,012m + 36 =>nC = 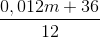 .103
.103
hay nC = 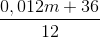 (kmol)
(kmol)
So sánh với 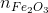 =
= 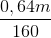 .103 = 4m (mol) hay 0,004m (kmol) => C dư
.103 = 4m (mol) hay 0,004m (kmol) => C dư
Theo pt (1): nC tham gia phản ứng = 3. 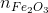 = 3. 0,004m = 0,012m (kmol)
= 3. 0,004m = 0,012m (kmol)
=>nCdư = 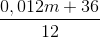 - 0,012m
- 0,012m
Hay mC dư = 0,012m + 36 – 0,144m = 36 – 0,132m
Theo phương trình (1): nCO = 3.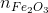 = 0,012m
= 0,012m
=>mCO = 0,012m.28 = 0,336 (kg)
Khối lượng thép tính được (áp dụng định luật bảo toàn khối lượng):
(1000 + m) – mCO = 1000 +m – 0,336m = 1000 + 0,664m Vậy ta có:
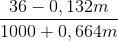 = 0,012 => m= 171,428 kg
= 0,012 => m= 171,428 kg