Tính thành phần phần trăm theo khối lượng của mỗi kim loại trong hỗn hợp A?

Câu hỏi và phương pháp giải
Nhận biếtTính thành phần phần trăm theo khối lượng của mỗi kim loại trong hỗn hợp A?
Đáp án đúng: B
Lời giải của Luyện Tập 247
Giải chi tiết:
PTHH: (Mg có tính khử mạnh hơn Fe nên phản ứng với CuSO4 xảy ra phản ứng theo thứ tự ưu tiên Mg phản ứng trước Fe)
Mg + CuSO4 → MgSO4 + Cu (1)
x x x x
Fe + CuSO4 → FeSO4 + Cu (2)
y y y y
MgSO4 + 2NaOH → Mg(OH)2↓ + Na2SO4 (3)
x x
FeSO4 + 2NaOH → Fe(OH)2↓ + Na2SO4 (4)
y y
Mg(OH)2 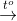 MgO + H2O (5)
MgO + H2O (5)
x x
4 Fe(OH)2 + O2 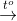 2Fe2O3 + 4H2O (6)
2Fe2O3 + 4H2O (6)
y 0,5y
Nếu A tác dụng hết với CuSO4 tạo ra muối thì khi nung kết tủa đến khối lượng không đổi thu được chất rắn D gồm ít nhất 2 oxit MgO và Fe2O3 (ngoài ra có thể có CuO do CuSO4 có thể dư).
Ta có: mD = mMgO + 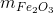 >mA = mMg + mFe = 0,51 gam
>mA = mMg + mFe = 0,51 gam
Đề ra: mD = mMgO + 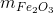 = 0,45 gam < mA = mMg + mFe = 0,51 gam
= 0,45 gam < mA = mMg + mFe = 0,51 gam
Vậy CuSO4 hết, A còn dư
TH1: Mg hết, Fe còn dư
Gọi số mol Mg và Fe phản ứng với CuSO4 là x và y; số mol Fe dư là z
Theo đề ra và PTHH ta có:
Chất rắn B thu được gồm Cu và Fe còn dư:
Hệ pt:
mA = 24x + 56.(y+z) = 0,51g
mB = 64x + (x+y) +56z = 0,69g
mD = 40x + 160.0,5y = 0,45g
=>x = y = z=3,75.10-3
Vậy thành phần khối lượng: %Mg = 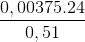 .100%= 17,65%
.100%= 17,65%
= 100% - 17,65 = 82,35%
TH2: Mg và Fe đều dư(Fe không có phản ứng)
Chất rắn D thu được chỉ có MgO => nMgO = 0,45:40 = 0,01125 mol
Theo phản ứng (1): 1 mol Mg phản ứng với khối lượng tăng: 64 – 24 = 40 gam
Vậy số mol Mg đã phản ứng là:
nMg phản ứng = 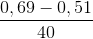 = 0,0045 mol ≠ 0,00125 mol (loại)
= 0,0045 mol ≠ 0,00125 mol (loại)